重磅喜讯!近日,微肽生物旗下子公司研发的“医用透明质酸钠凝胶”(注册证编号:湘械注准20252140828)正式获得湖南省药品监督管理局颁发的二类医疗器械注册证。
该产品针对不同临床与消费场景,创新性地推出六种差异化剂型与包装系统,标志着企业在创面护理领域的产品研发与临床适配能力迈上新台阶。
医用透明质酸钠凝胶:临床价值显著,应用场景广泛
医用透明质酸钠凝胶作为一种重要的医疗器械,其主要成分为透明质酸钠。透明质酸钠是一种天然存在于人体结缔组织、眼球玻璃体及关节液中的高分子多糖,具有优异的保湿性、润滑性和生物相容性。在医疗领域,医用透明质酸钠凝胶被广泛应用于多个方面:
1、创面修复与皮肤保护:其良好的保湿和屏障功能,使其成为烧伤、皮肤裂伤、手术切口等创面护理的理想选择。通过维持创面湿润环境,促进细胞迁移和再生,加速组织修复过程,同时减少疤痕形成。
2、眼科手术辅助:在白内障手术、角膜移植等眼科手术中,医用透明质酸钠凝胶用于维持眼内空间,防止组织损伤,提高手术安全性和成功率。
3、关节炎治疗:作为关节注射液,透明质酸钠凝胶能有效改善关节润滑,缓解疼痛和炎症,促进软骨修复,尤其适用于骨关节炎患者。
4、美容注射材料:凭借其良好的填充效果和安全性,透明质酸钠凝胶被广泛应用于面部填充、皱纹改善等医疗美容领域。

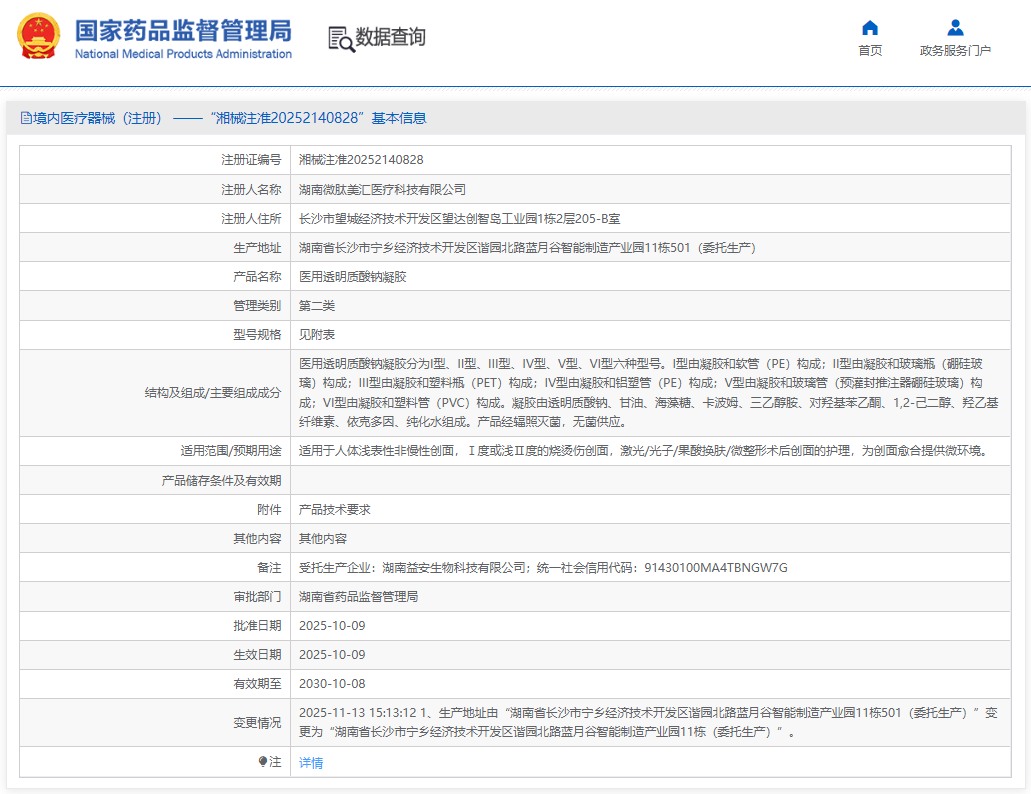
微肽生物研发的医用透明质酸钠凝胶——适用于人体浅表性非慢性创面,Ⅰ度或浅Ⅱ度的烧烫伤创面,激光/光子/果酸换肤/微整形术后创面的护理,为创面愈合提供微环境。
【结构组成】凝胶由透明质酸钠、甘油、海藻糖、卡波姆、三乙醇胺、对羟基苯乙酮、1,2-己二醇、羟乙基纤维素、依克多因、纯化水组成。产品经辐照灭菌,无菌供应。
【注册证编号】湘械注准20252140828
六大剂型设计,覆盖多元使用场景
本次获批产品按包装系统分为I至VI型,充分考虑了医疗机构、美容诊所及家庭护理等不同场景的操作需求:
I型(软管装) 与 IV型(铝塑管装) 便于局部涂抹,适合小面积创面护理;
II型(玻璃瓶装) 与 III型(塑料瓶装) 适用于需要多次取用的临床环境;
V型(预灌封玻璃推注器) 实现无菌直接推注,满足激光、微整形术后精准给药需求;
VI型(塑料管装) 兼具便携性与经济性,拓展日常护理使用场景。

微肽生物旗下-湖南微肽生物医药有限公司作为国内领先的二类、三类医疗器械研发与生产一体化企业之一,始终致力于为品牌方提供高品质的医疗器械解决方案。此次获批的医用透明质酸钠凝胶,是公司研发团队多年潜心研究的成果。
在研发过程中,微肽生物严格遵循国家医疗器械相关法规和标准,从原料采购、生产过程监控到成品检验,每一个环节都精益求精。公司采用先进的生产工艺和设备,确保产品的纯度和稳定性。同时,通过多中心临床试验验证产品的安全性和有效性,为临床应用提供有力保障。
获批背后:严格监管与技术创新并重
二类医疗器械的注册审批过程极为严格,需要经过国家药品监督管理局的全面审查。微肽生物此次获批的医用透明质酸钠凝胶,在注册申报过程中,提交了详尽的技术文件、安全风险分析报告、产品性能自测报告、注册检验报告以及临床试验资料等核心文件。
在技术审评阶段,国家药品监督管理局医疗器械技术审评中心对产品的安全性、有效性和质量可控性进行了全面评估。经过严格的审查和现场核查,最终确认微肽生物的医用透明质酸钠凝胶符合二类医疗器械的注册要求,准予注册。


市场展望:满足多元需求,引领行业升级
随着医疗技术的不断进步和人们健康意识的提高,医疗器械市场需求持续增长。医用透明质酸钠凝胶作为一种安全有效的辅助治疗产品,其市场前景广阔。微肽生物此次获批的医用透明质酸钠凝胶,不仅丰富了公司的产品线,更为公司开拓市场提供了有力支持。
未来,微肽生物将继续秉承“创新驱动、品质为先”的发展理念,加大研发投入,不断优化产品性能,提升服务质量。同时,公司将积极与国内外科研机构合作,推动透明质酸钠应用技术的升级和创新,为临床提供更多高品质、安全有效的医疗器械产品。


专业定制服务,助力品牌快速腾飞
至今为止,微肽生物已累计持有超100+二类医疗器械产品注册证,资质广审齐全,覆盖术后修护、创面护理、疤痕管理、止血材料、私密护理、口腔健康等多个细分领域。
5大现代化生产基地,万级无菌生产车间,配备专业研发团队和先进的自动化生产设备,为品牌方提供全方位OEM定制支持,满足不同品牌的个性化需求;产能强大,高效响应大批量订单,供货稳定,三天急速出货,市场全渠道供货无忧。
专业OEM服务让您轻松入局!欢迎品牌方、渠道商、医疗机构等广大合作伙伴,依托我们成熟的产品矩阵,精准布局多元赛道,共拓市场新版图!


